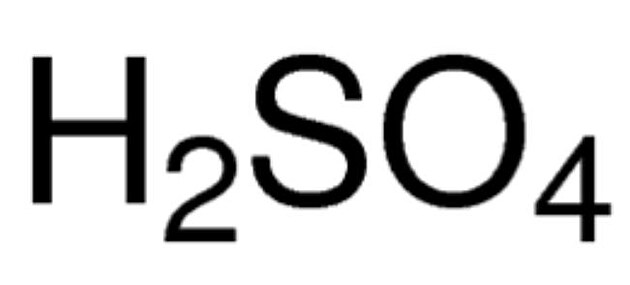- Napište nám
- Kontakty
- Reklama
- VOP
- Osobní údaje
- Nastavení soukromí
- Cookies
- AV služby
- Kariéra
- Předplatné MF DNES
Kterak zadarmo udělat VŠ zkoušku z chemie
Musíte ve cvičení vyrušovat, zlobit a nedávat pozor. Pak vás totiž vyučující vyvolá a musíte k tabuli. V tomto případě to bylo na reakci kyseliny sírové H2SO4 a s louhem sodným NaOH. A zadání bylo spočítat kolik gramů NaOH musíme použít na 98 gramů kyseliny sírové, aby se spotřebovaly obě suroviny a dostali jste čistý síran sodný Na2SO4 a vodu H2O. K tomu potřebujete znát molekulové váhy obou původních sloučenin.
Je to výpočet tak na 10 minut, když ony váhy neznáte, tedy přesněji neznáte atomové váhy (korektně relativní atomové hmotnosti) jednotlivých prvků a musíte je najít v tabulkách. Kyslík má zhruba 16, vodík 1, síra 32, sodík 23. Takže molekulová váha (pardon hmotnost) kyseliny sírové je 2x1 + 32 + 4x16 = 98, molekulová váha hydroxidu sodného je 23 + 16 + 1 = 40. Ale s jednou molekulou sírovky reagují dvě molekuly NaOH. Z toho je jasné, že na 98 gramů kyseliny sírové musíte použít 80 gramů NaOH.
Takže na tenhle úkol jsem byl vyvolán, tak jsem šel k tabuli a rovnou napsal výsledek. A to mi vyneslo onu zkoušku zdarma. Třída totiž následně několik minut hledala v tabulkách a počítala výsledek a došla ke stejnému. Nebylo to ale žádný zázrak, ani genialita, ale měl jsem právě za sebou čerstvě chemickou průmyslovku, obor analytická chemie a to zrovna anorganická. Proto jsem takových příkladů počítal tisíce a tisíce a atomové hmotnosti nejčastějších prvků jsem si pamatoval. A sečíst pár čísel netrvalo delší dobu, než na cesta ze zadní lavice k tabuli.
Jan Fikáček
Proč jsou izraelská média daleko méně proizraelská než česká?

Jan Fikáček
Solvay institut - Einstein, Schrödinger, Planck, Heisenberg, Bohr atd.

Jan Fikáček
Nahraďte svou ženu a děti umělou trpělivostí (inteligencí?)!

| Další články autora |

Chcete, aby vaše děti měli v dospělosti bohatství? Přečtěte si, jak na to!
Správné finanční návyky a dovednosti vznikají právě v dětství. Mnoho dětí je přijímá přirozeně od svých rodičů, kteří jsou pro děti velkým vzorem....
Střední školy
Nepřehlédněte
- Na jednání o míru nepřijdeme, vzkázali Rusové. Švýcaři je ani nezvali
- Konec snu o medaili. Hokejová osmnáctka prohrála ve čtvrtfinále MS se Slováky
- Basketbalisty Barcelony čeká rozhodující pátá bitva s Olympiakosem
- Pavel zkritizoval všechny. Nefér jsou Babišova slova i kampaň SPOLU, míní
- O menopauze musíme mluvit, burácela herečka Halle Berry před Kapitolem
- Lehečka postoupil v Madridu do semifinále, zraněný Medveděv vzdal
- Hvězdy NHL ozáří MS v Česku. Přijedou Hedman, Karlsson, Bedard či Tkachuk
- Triumf v řepkovém poli. Nervózní Ústí zlomilo divácký rekord i rivala z Děčína