- Napište nám
- Kontakty
- Reklama
- VOP
- Osobní údaje
- Nastavení soukromí
- Cookies
- AV služby
- Kariéra
- Předplatné MF DNES
Chemie pod víčkem (2) - všestranný hrdina pektin
Stejně jako škrob nebo celulóza jsou pektiny komplikovanými cukry, pochází tedy z říše rostlin.
Chemická látka pektin byla objevena v roce 1790 vědcem Vauquelinem. Později ji Braconnot charakterizoval jako složku ovocného materiálu, která je zodpovědná za tvorbu gelu. Poprvé ji také pojmenoval názvem pektin, pocházejícím z řeckého slova "srážet se, tuhnout".
O sto let později zjistil jiný věděc, Smolenski, že pektin může být tvořen polymerní kyselinou galakturonovou. V roce 1930 odhalili Meyer a Mark řetězcovou formu molekuly pektinu a v roce 1937 už byl znám chemický vzorec, za který vděčíme jiným dvěma kolegům, Schneiderovi a Bockovi.
Pektiny se syntetizují prakticky ve všech vyšších suchozemských rostlinách. Nalézt se dají v pevných složkách rostlin, tedy ve stoncích, květech, listech apod. Hrají tu zpevňující a vodoregulační úlohu. Aby nebyla situace tak jednoduchá, liší se obsah pektinu, ale také jeho složení tzv. “kus od kusu”. Záleží nejen na typu, ale také na stáří a stupni zralosti rostlinného materiálu.
Všeobecně se dá říci, že hodně pektinu obsahují ty části rostlin, která jsou houževnaté a tvrdé.
Obsah pektinů v ovoci
Platí tedy, že čím pevnější ovoce, tím vyšší je v něm obsah pektinu. Jablka, citrusové plody a kdoule mají výrazně více pektinu než měkké ovoce, jako jsou jahody a maliny. Platí také, že sladké ovoce obsahuje přirozeně více pektinu než kyselé. To se může zdát na první pohled zvláštní, vždyť víme, že právě kyselé ovoce dobře želíruje, na první pohled by tedy mělo mít více pektinu.
Vysvětlení role kyseliny v želé jste si mohli přečíst v minulém blogu. Kyselina neutralizuje anionty, které se nacházejí na povrchu pektinové molekuly - a které způsobují, že se tyto molekuly vzájemně odpuzují, takže nedokážou vytvořit stabilní trojrozměrnou síť (pevný gel). V přítomnosti kyseliny se tedy zvyšuje schopnost želírování. A to by vlastně mohlo vysvětlit jeho vyšší obsah ve sladkém ovoci. Příroda prostě potřebuje k vytvoření stejného efektu více pektinu.
Ovoce má nejvíce pektinu krátce před tím, než je zcela zralé. Nejlepší džemy a marmelády tedy vyrobíte z lehce nezralých plodů.
Málo pektinu mají banány, jahody, bezinky, třešně, mango a rebarbora. Naopak vysoké množství pektinu se nachází v citrusových plodech, jablcích, kdoulích, rybízu a angreštu.
Obsah pektinu v meruňkách, broskvích, nektarinkách, švestkách, sušených švestkách, malinách a mirabelkách není tak vysoký.
Aby se želírování podařilo i u těch druhů ovoce, které přirozeně moc pektinů nemají, může se k nim přidávat takové ovoce, které ho má nadbytek. Alternativou je přidání umělého pektinu, vyrobeného chemicky.
“Chemický pektin”
Ročně se na celém světě vyrobí přibližně 40 000 tun pektinu. Získává se z rostlinných surovin s vysokým obsahem pektinu, jako jsou jablečné, citrusové nebo řepné výlisky, tedy odpad z jiných potravinářských výrob.
A aby ani tady nebyla situace moc jednoduchá - existují různé úpravy a metody extrakce, které zajišťují výrobu různých pektinových typů s různými vlastnostmi.
Princip je ale u všech postupů podobný: nejprve probíhá extrakce látek, rozpustných ve vodě (pomocí horké vody). Poté se od nich oddělí samotný pektin vysrážením z vodného roztoku pomocí etanolu nebo acetonu. Bílý prášek, který přidáváte k ovocné hmotě při zavařování, už má tedy za sebou pravou a nefalšovanou alkoholickou párty.
Poté se materiál odstřeďuje a promývá, aby se zajistila jeho chemická čistota.
Pak ho čekají další chemické proměny, tzv. modifikace. Ty už mohou probíhat různými způsoby. Jedním z nich je například kontakt s amoniakem (čpavkem). Vznikají při něm amidované pektiny, které nesou označení E440ii.
Další filtrací, mytím a sušením se získá bílý až šedavý pektinový prášek. Podle toho, pro jaké využití je určen, se ještě míchá s dalšími látkami, jako cukr, pufrovací látky pro regulaci hodnoty pH nebo konzervanty.
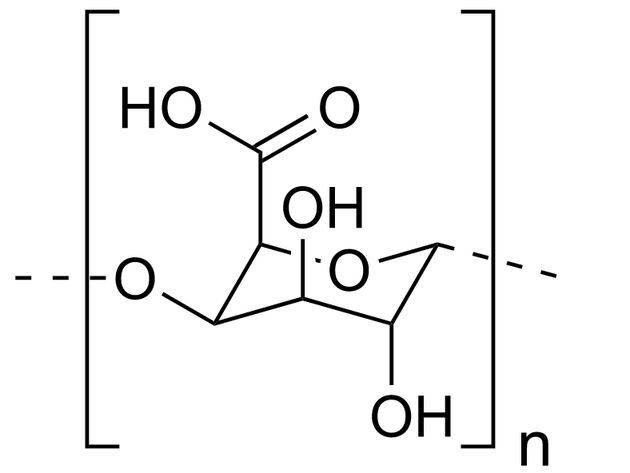
Všechny takto vyrobené pektiny patří do chemické skupiny polysacharidů. Jsou to tedy komplikované polymery, jejichž hlavní složkou (nejméně 65 % hmotnosti) je kyselina ?-D-galakturonová.
Viskozita roztoků pektinů (tedy jejich želírovací schopnosti) je závislá na parametrech procesu, kterými se vyrobily. Podobně záleží také na kyselosti systému, přítomnosti různých
pevných látek nebo rozpouštědel, na přítomnosti kovových iontů, koncentraci samotného pektinu a samozřejmě také teploty.
Celá situace je komplikovaná, protože se všechny tyto parametry vzájemně ovlivňují. Tato oblast organické chemie dává vědcům hodně prostoru k výzkumu. Není tedy divu, že v bylo v posledních desetiletích na toto téma provedeno velké množství studií.
Ty hlavní proběhly už v 50. letech 20. století a poté znovu v 90. letech 20. století. Poslední dobou se výzkum soustředí spíše na chemické modifikace pektinu.
Konkrétní využití pektinu
Pektin se dá dnes nalézt nejen v potravinách, ale také ve výrobcích farmaceutického průmyslu nebo v kosmetice - všude tam, kde se z různých důvodů uplatní želírující, zahušťující, anebo stabilizující látky.
Nejznámější a nejoblíbenější je samozřejmě při domácí výrobě želé, džemů a marmelád, cukrovinek, pekařských výrobků, ke stabilizaci nápojů a v mléčných výrobcích. Pektiny, stejně jako agar-agar, karagenan nebo kyselina alginová, mohou sloužit jako čistě rostlinná náhrada želatiny.
V EU je pektin schválen jako přísada E440, bez omezení maximálního množství (quantum satis), které může potravina obsahovat.
Zajímavé využití pektinů je způsobeno jejich schopností působit jako komplexotvorná látka - a pomáhat při detoxikaci v případě otravy těžkými kovy. Snižuje prý také hladinu cholesterolu v krvi. Bílého prášku, kterým si pomáháme při domácím zavařováním ovoce, se tedy nemusíme bát. I když při výrobě prošel všemožnými stupni chemických proměn, není nebezpečný - a pro někoho může být dokonce … svým způsobem i zdravý.
Zdroj: https://www.db-thueringen.de/servlets/MCRFileNodeServlet/dbt_derivate_00049877/disskayser.pdf
Dana Tenzler
Co způsobuje barvu minerálů (4) - klamání tělem a přibarvování reality

Dana Tenzler
Co způsobuje barvu minerálů (2) - proč jsou vlastně děti zlobivé?

| Další články autora |

Inspektor/ka – oblast vigilance zdravotnických prostředků
Státní ústav pro kontrolu léčiv
Praha
Střední školy
Nepřehlédněte
- Sudetští Němci pořádají třídenní sjezd. Zúčastní se český velvyslanec
- Holubí balet a zajíc v úprku. Lázeňské lesy se pochlubily fotkou z mýtiny
- Nečas gólem otevřel skóre, výhru a postup ale nakonec slavili Rangers
- Alaphilippe se už zase směje: Mrtvý jsem nikdy nebyl, chtělo to trpělivost
- Ústí zruší zahrádkářskou kolonii, kde uhořeli čtyři lidé. Chaty stojí načerno
- Nájemné ve velkých městech dál zdražuje, nových domů s pronájmy vzniká minimum
- Panasonic překvapil, jeden opuštěný operační systém nahradily dva nové
- RECENZE: Matnému filmu o Amy Winehouse by mnohem víc slušela televizní obrazovka